- 投稿邮箱:qizhixmt@126.com
国家药监局医疗器械监管司党支部认真开展党史学习教育,结合医疗器械监管实际,扎实开展“我为群众办实事”实践活动,努力做到党建和监管工作双促进、双提升。
以“我为群众办实事”为切入点,谋实事、开新局
强化党史学习教育与监管业务工作深度融合,注重学习成果转化,更好地发挥党支部战斗堡垒作用和党员先锋模范作用。
立足实际,谋事求真务实。医疗器械关乎公众身体健康和生命安全。器械监管司深入贯彻落实“四个最严”要求,强化风险管理,立足我国医疗器械监管实际,紧盯社会关注、群众关心的热点问题,聚焦高风险产品和疫情防控常态化下医疗器械质量监管,聚焦人民群众新期待,组织全系统开展医疗器械风险隐患排查治理。
排查治理,加强监督检查。组织对无菌和植入性医疗器械、疫情防控类医疗器械等产品,以及投诉举报频发、监督检查和产品检验不合格等重点企业及产品加大风险隐患排查力度。组织企业自查,排除安全隐患。组织监督检查,严厉查处违法违规行为。今年以来,各地累计监督检查医疗器械生产企业4230家次,排查经营企业和使用单位11万余家,责令整改企业5035家,立案查处812家,约谈企业152家。组织对国家集采冠脉支架、新冠病毒疫苗配套使用一次性无菌注射器等重点产品督导检查,强化医疗器械质量监管。
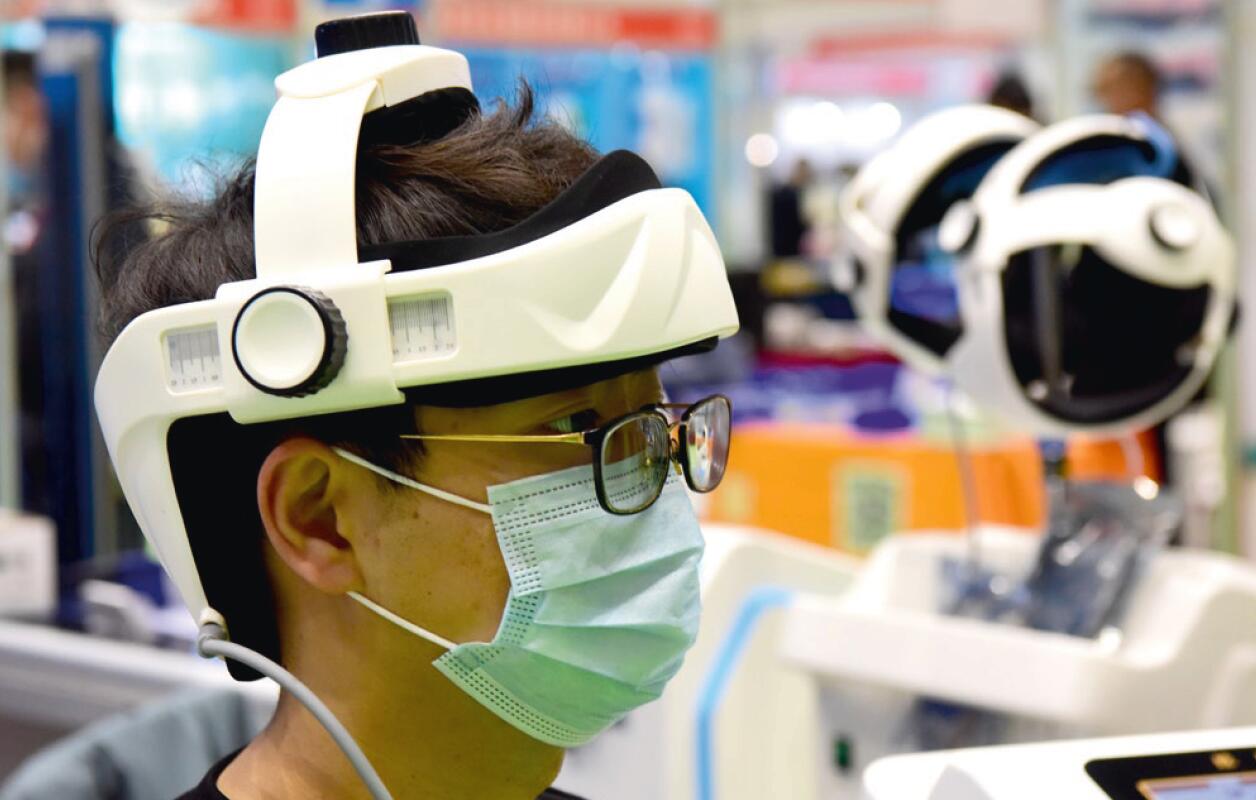
>> 3月11日至13日,2021年春季中原医疗器械展览会在河南郑州国际会展中心举行,来自全国各地1000余家医疗器械参展商到会参展。
优化准入,推进“放管服”。认真总结监管经验,充分征求业内相关部门、行业协会和企业意见,拟对部分安全性、有效性不受流通过程影响的第二类医疗器械,免于经营备案。拟将血压计、血糖试纸等13个第二类医疗器械产品纳入免于经营备案目录,力争尽快发布施行,为企业营造良好营商环境,为百姓购买、使用医疗器械提供方便。
以加强药品监管能力建设为支撑点,强基础、促提升
坚决贯彻落实党中央、国务院决策部署,立足新发展阶段、贯彻新发展理念、构建新发展格局,抓住机遇,应对挑战,加快提升药品监管治理体系和治理能力,助力发展、服务大局。
深刻把握监管事业发展的历史机遇期。建党百年之际,新修订的《医疗器械监督管理条例》和国务院办公厅《关于全面加强药品监管能力建设的实施意见》相继发布,从筑牢法规制度基础,提升标准、监测、检验技术支撑,强化监管执法体系联动等方面着手,作出一系列重大部署,充分体现了党中央、国务院对药品监管工作的高度重视。器械监管司将深刻把握历史机遇,推动医疗器械监管体系和能力的科学化、法治化、国际化、现代化发展。
加快推进监管体系和能力现代化。以上率下,学习总结经验,器械监管司将带领全系统全面加强医疗器械质量监管,积极保障人民群众用械安全和用械需求,加强器械监管体系和能力建设、促进行业高质量发展,全面提升药品监管体系和监管能力现代化。近年来,我国医疗器械产业快速成长,心血管支架、监护仪等一大批国产医疗器械基本实现进口可替代。但部分高端医疗器械和一些关键核心零部件、材料存在短板。器械监管司将进一步推动医疗器械创新发展,勇做健康中国战略、高质量发展事业的担当者、实干者,助力国内国际市场双循环发展,锤炼具有全球竞争力的产品质量和监管能力。
以人民对医疗器械的新期待为落脚点,保安全、助发展
在“十四五”开局之年,医疗器械监管工作要紧紧围绕保障群众用械安全,以让人民群众用械需求得到更好的满足,作为一切工作的出发点和落脚点,进一步提升质量安全保障水平,推动医疗器械高质量发展。
加大政策宣贯科普力度。全力做好新修订《医疗器械监督管理条例》宣贯培训,加大《关于全面加强药品监管能力建设的实施意见》政策解读,充分利用宣贯培训会、研讨会、报刊等载体,面向医疗器械注册人、备案人、行业协会、社会公众广泛宣传,加强安全用械科普知识宣传。
加速推进法规制度建设。落实新修订的《医疗器械监督管理条例》规定,贯彻医疗器械注册人全生命周期质量管理制度,积极做好医疗器械生产、经营监管等部门规章修订,认真研究出台医疗器械管理技术指南及规范性文件,组织研究注册人和生产企业质量管理体系年度自查报告编写指南、注册人委托生产协议指南文件,医疗器械重点监管目录等,进一步完善上市后监管法规制度体系。
加强风险隐患排查治理。注重风险会商研判,深入排查医疗器械质量安全隐患,及时发现并消除苗头性、倾向性问题,保障产品质量安全。监督医疗器械注册人落实医疗器械全生命周期质量安全责任。督导地方各级药品监管部门加强协同配合,形成信息通畅、衔接有序、协作有力的监管合力。
强化监督检查执法力度。针对群众关心、社会关注的投诉举报,对舆情频发的医疗器械以及无菌植入性医疗器械、国家集中带量采购医疗器械、创新医疗器械等产品加大监督检查频次,对发现的违法违规行为重拳出击,切实做到查办一案、警示一片,形成震慑。
深化产品抽验和不良事件监测。持续开展医疗器械不良事件监测,及时发现和分析可能存在的风险,并采取有效控制措施。加强医疗器械检验检测机构建设,特别是尽快提升各地本区域疫情防控医疗器械等重点产品的检验检测能力。针对高风险产品、重点企业以及重点品种,进一步加强抽检工作力度。
抓好监管体系和队伍能力建设。注重强化监管基础建设和信息化、现代化监管手段建设,进一步完善监管数据,加强监管信息系统使用和数据对接,强化国家、省、市、县监管信息协调互通,提高监管效能。加强职业化专业化检查员队伍建设,加大兼职检查员认定力度。确定一定数量的检查员实训基地,对检查员进行分类分级培训和管理,以适应新形势下检查工作需要。守住质量安全底线,更好保障人民群众用械安全,让人民群众用械需求得到更好满足。
(来源:《旗帜》2021年第6期)
( 编辑:孙丽 送签:张成付 签发:张桃英 )
中央和国家机关工委旗帜杂志社版权所有 人民网 中国共产党新闻网承建 版权声明
转载请注明来源,京ICP备18060497号-1,京公网安备11010102006249号,互联网新闻信息服务许可证10120170065,信息网络传播视听节目许可证0120672
违法和不良信息举报电话:(010)64068010
